2014年ADR報告發布:基藥平穩 中藥注射劑基層“反應”多
日期:2015/7/25
中藥注射劑與其他藥品聯合使用有可能增加安全風險,應慎重考慮藥物相互作用以及與中藥注射劑的間隔時間、輸液容器的清洗等問題。
日前,國家食品藥品監督管理總局(CFDA)發布《國家藥品不良反應監測年度報告(2014年)》。報告顯示,我國藥品不良反應報告覆蓋面拓寬,發現和收集藥品不良反應信息的能力增強,公眾用藥安全意識進一步提升。
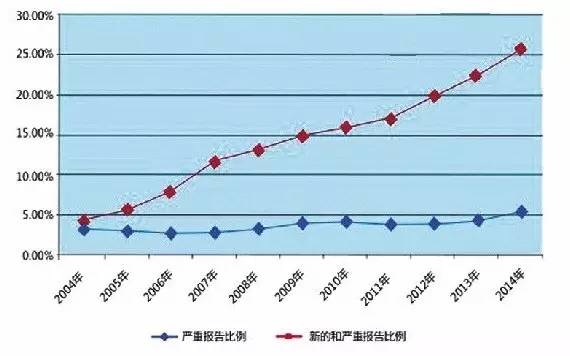
2014年,國家藥品不良反應監測網絡共收到藥品不良反應/事件報告132.8萬余份,比2013年增長0.8%。其中,新的和嚴重的藥品不良反應/事件報告34.1萬份,占同期報告總數的25.7%。以縣為單位,藥品不良反應報告覆蓋率達到94.4%,全國每百萬人口平均報告數量達到991份。
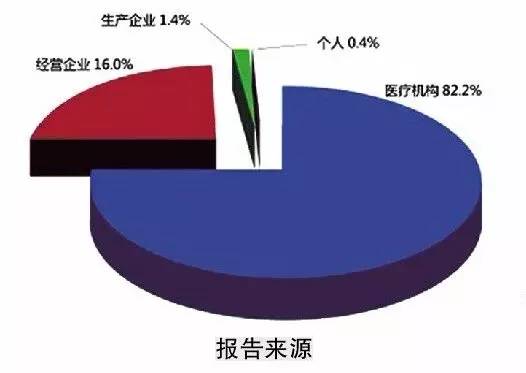
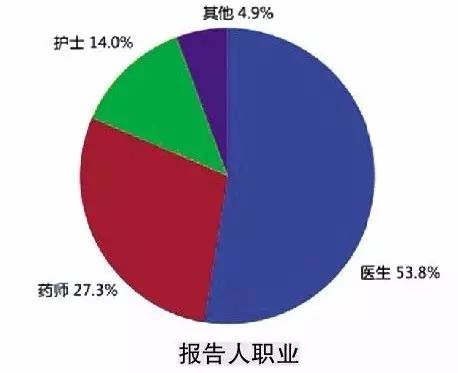
統計分析顯示,醫療機構仍是不良反應報告的主要來源,占報告數量的82.2%,藥品經營企業的報告占16.0%,藥品生產企業的報告占1.4%,個人及其他來源的報告占0.4%。與2013年相比,醫療機構報告增長明顯,藥品生產企業報告比例與既往持平,經營企業報告比例繼續下降。
據悉,近日CFDA發布了《藥品不良反應報告和監測檢查指南(試行)》,以推動藥品生產企業實施藥品不良反應報告和監測制度,指導各級食品藥品監管部門對企業開展藥品不良反應報告和監測工作的檢查。
基本藥物狀況平穩
自實施國家基本藥物制度以來,基本藥物的不良反應是監測的重點之一。據統計,2014年全國藥品不良反應監測網絡共收到國家基本藥物的不良反應/事件報告52.0萬例(占2014年總體報告的39.2%),其中嚴重報告2.9萬例,占5.6%。總體上看,2014年國家基本藥物安全狀況繼續保持平穩。
據介紹,《國家基本藥物目錄(基層醫療機構配備使用部分)》(2012版)化學藥品和生物制品部分,共分25個類別,約317個品種。2014年全國藥品不良反應監測網絡共收到國家基本藥物中化學藥品和生物制品不良反應/事件報告443,300余例次,其中嚴重報告28,400余例次。2014年國家基本藥物化學藥品和生物制品報告按類別統計,報告數量排名前5位的分別是抗微生物藥,心血管系統用藥,抗腫瘤藥,消化系統用藥,鎮痛、解熱、抗炎、抗風濕、抗痛風藥,占基本藥物化學報告的74.1%。化學藥品(含生物制品)報告數量排名前五位的品種均為抗微生物藥,分別是左氧氟沙星、頭孢曲松、頭孢呋辛、頭孢他啶和青霉素。主要不良反應表現為:皮疹、惡心、瘙癢、嘔吐、頭暈、頭痛、過敏反應等。
《國家基本藥物目錄(基層醫療衛生機構配備使用部分)》(2012版)中成藥部分涉及內科用藥、外科用藥、婦科用藥、眼科用藥、耳鼻喉科用藥、骨傷科用藥6大類共203個品種。2014年全國藥品不良反應監測網絡共收到不良反應/事件報告91,400余例次,其中嚴重報告4,670例次。
其中,內科用藥報告總數占到基本藥物中藥類總體報告數量的85.4%。據分析,內科用藥占比較大可能與內科用藥臨床使用量大,且基本藥物目錄中中藥注射劑都屬于內科用藥有關。內科用藥報告排名前五位的分別是祛瘀劑、溫里劑、開竅劑、清熱劑、解表劑,此五類藥品報告占到內科用藥報告數的76.5%。中成藥注射劑排名前五位的品種分別是清開靈注射液、參麥注射液、血塞通注射劑、血栓通注射劑和丹參注射液。中藥注射劑主要不良反應表現多為皮疹、瘙癢、胸悶、心悸、惡心、過敏反應、頭暈等,中成藥口服制劑主要不良反應表現多為惡心、腹瀉、皮疹、腹痛、瘙癢、嘔吐、頭暈、胃不適、頭痛、口干、腹脹、過敏反應等。
據悉,2014年CFDA根據藥品不良反應監測風險信號,組織對胞磷膽堿鈉注射劑、硫酸鎂注射液等基本藥物開展安全性評價,并采取了相應風險控制措施。
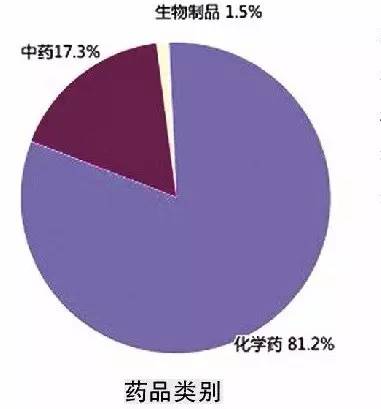
在對2014年藥品不良反應報告進行按涉及藥品類別統計發現,化學藥占81.2%、中藥占17.3%、生物制品占1.5%。抗感染藥報告數量仍居首位,占化學藥的46.2%,較2013年降低了1.4個百分點,報告比例已連續5年呈下降趨勢。心血管系統用藥占化學藥的10.2%,較2013年上升了0.2個百分點,且連續5年呈上升趨勢。
CFDA藥化監管司稽查專員張愛萍說,這說明我國對抗感染藥采取的例如發布《抗菌藥物臨床應用指導原則》等措施取得一定實效,建議臨床醫生繼續按照這些原則合理使用抗感染藥,降低使用風險。
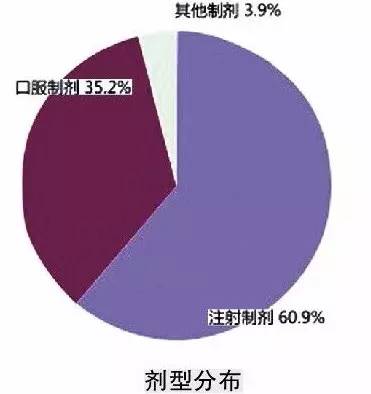
從涉及藥品劑型看,注射劑報告數在2014年比例仍然較高,占60.9%,較2013年提高2.2個百分點;口服制劑比例占35.2%。
其中,中藥注射劑依然值得關注:2014年全國藥品不良反應監測網絡共收到中藥注射劑報告12.7萬例次,其中嚴重報告占6.7%。與2013年相比,中藥注射劑報告數量增長5.3%,高于總體報告增長率;嚴重報告數量增長26.0%,與總體嚴重報告增長情況基本一致。
通過對2014年中藥注射劑病例報告數量排名前20名藥品的用藥單位情況分析顯示,基層醫療衛生機構(含衛生院、衛生所、個人診所等)使用中藥注射劑發生不良反應報告多于其他醫院報告,例如清開靈注射劑相關的不良反應報告有75%來自基層衛生醫療機構。
據分析,2014年中藥注射劑安全狀況與全國整體情況基本一致,嚴重報告增長幅度略低于全國整體報告增長幅度,提示可能與藥品監管部門、藥品生產及使用單位采取措施持續推動合理用藥以及開展相關宣傳培訓有關。
北京醫院藥劑科主任胡欣表示,中藥注射劑與其他藥品聯合使用有可能增加安全風險,提醒臨床醫師須注意單獨使用中藥注射劑,禁忌與其他藥品混合配伍使用;如確需要聯合使用其他藥品時,應慎重考慮藥物相互作用以及與中藥注射劑的間隔時間、輸液容器的清洗等問題。
據介紹,根據2014年藥品不良反應監測數據和評估結果,CFDA對發現存在安全隱患的藥品及時采取不良反應信息通報、藥物警戒、修改說明書等相應風險控制措施,以保障公眾用藥安全。
信息來源:醫藥經濟報
|