【信息會智庫資料】2014年全球暢銷藥Top50及國產競品分析
日期:2015/10/23
第27屆全國醫藥經濟信息發布會獨家特約撰稿人
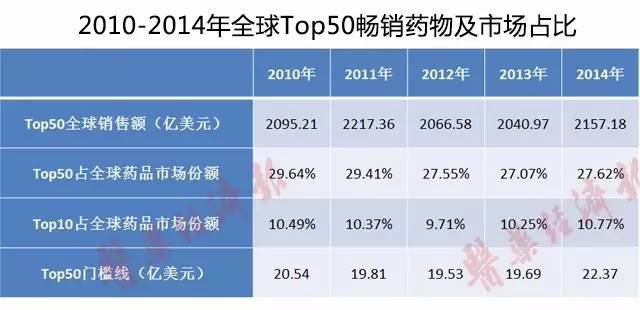
根據EvaluatePharm的統計顯示,2014年全球暢銷藥物50強總銷售額達到了2157.18億美元,占全球處方藥及OTC藥物市場總額的27.62%,相比2013年有所提升,該比例在2010-2014年均保持在27%以上。其中前十強占總體藥物市場的10.77%,該比例自2012年低于10%以下,為9.71%外,歷年均在10%以上。可以看出全球暢銷藥50強對世界藥物市場格局的影響巨大。受多種因素的而影響,傳統重磅藥物的市場主導地位正在不斷削弱,暢銷藥物對全球銷售額的貢獻率處于下降趨勢。
排行榜中第50位的藥物是澤珂(Zytiga),2014年銷售額為22.37億美元,這也是2014年全球暢銷50強的門檻線,自2011年的門檻線跌至19.81億美元以來,2014年又重新回到20億美元的準線上。
2014年全球暢銷藥物前10強銷售總額達841.67億美元,占前50強的比重為39.14%,較2013年有所提升。2014年前十強藥物的排名因Sovaldi的加入而劇烈震蕩。吉利德的抗丙肝新藥Sovaldi(sofosbuvir)于2013年年底在美國批準上市,隨后2014年1月歐盟也批準臨床使用,這是世界上首個純口服抗丙肝藥物,其2014年全球銷售額達到102.83億美元,位居榜單第二,同比2013年的增長率更是高達7275%。
自2012年阿達木單抗“修美樂”榮居榜首后,已連續三年蟬聯冠軍,2014年銷售額為128.9億美元,得益于最近FDA批準的第7個適應癥和價格上漲,修美樂在2014年的全球銷售額比前一年上漲了17%。因為修美樂銷售基數較大,其2014年較2013年的絕對漲幅高達18.76億美元,僅僅漲幅就相當于一個重磅產品的銷售額。Sovaldi的橫空出世使得榜單上的其他藥物名次逐個后移,其中GSK的哮喘治療藥物舒利迭(Seretide)下降的更多,由第4降至第7,2014年全球銷售額同比下降15%。舒利迭銷售下降的原因更多是由于仿制藥競爭壓力、臨床可替代藥品兩大主要因素。邁蘭公司已在英國市場上推出舒利迭的第一只仿制產品,提供給成年哮喘患者使用。在哮喘和COPD治療領域,來自替代產品如阿斯利康的信必可(Symbicort)和默沙東的順爾寧(Singulair)的競爭也對舒利迭構成極大威脅,這些因素導致舒利迭的市場份額逐步被吞噬。
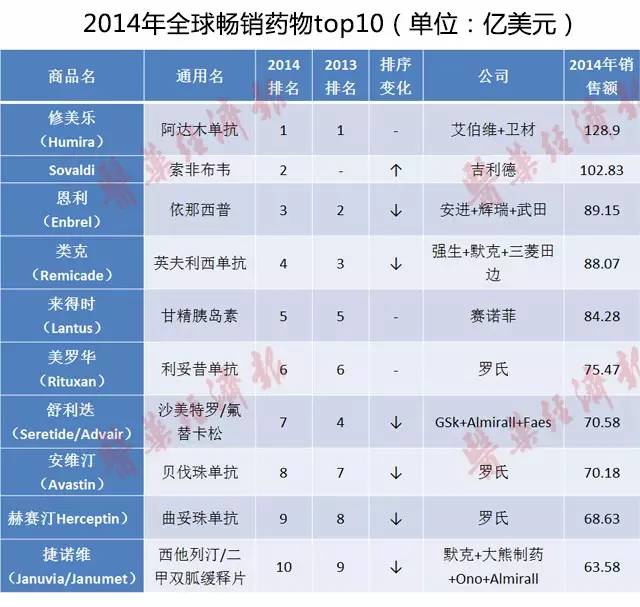
生物醫藥技術的發展使得生物藥物在疾病治療中取得了更多的突破,近年來生物藥物的增長一直引領行業發展。立普妥之后最暢銷的藥物是艾伯維的修美樂,成為首個年度銷售額過百億美元的生物藥。2014年全球Top50藥物中,生物技術藥共有22個,共創造了1058.24億美元的市場價值,銷售額占比49.05%,已占據半壁江山。而在Top10中,生物技術藥物達7個,銷售額占比71.84%,生物技術藥物已經占據主導地位,其中恩利(Enbrel)與來得時(Lantus)屬于生物技術重組產品,而修美樂(Humira)、類克(Remicade)、美羅華(Rituxan)、安維汀(Avastin)、赫賽汀(Herceptin)都屬于單抗類別。
但這些生物藥大部分將在2020年因失去專利保護,而丟掉市場排他性地位,將面臨生物類似物的激烈競爭。從2020年的銷售預測情況來看,除了修美樂勉強保持市場穩固之外,其余生物藥市場份額均有下降。賽諾菲的來得時下降達9%,因為在2015年,基礎胰島素來得時在歐洲將面臨禮來生物類似藥的競爭。到2020年,類克的銷量將下降5%,在2013年歐盟批準了韓國的Celltrion公司的Remsima和伊利諾斯州的Hospira公司的Inflectra,這是兩個仿制版的英夫利西單抗,這是全球首個單抗類生物仿制藥,在業內引起反響較大。這也意味著強生和默沙東的產品也將直接地暴露在生物類似藥的競爭中。
2014年全球處方藥市場銷售額領先的企業入圍暢銷藥50強榜單方面,強生入圍的產品數最多,為6個。安進與輝瑞分別入圍5個品種,其次是諾華、羅氏、默克各有4個,賽諾菲、阿斯利康、吉利德各有3個。

從2014年Top50暢銷藥物的治療類別看,暢銷藥物由傳統的高膽固醇高血壓等領域快速切入到時下患病率最高的腫瘤領域;腫瘤、關節炎、糖尿病、呼吸系統等是發病率靠前的疾病領域,這也與暢銷藥物治療類別重合,但唯一例外的是細菌感染類,雖然發病率不低,但抗菌藥并未出現在榜單。在2014年全球暢銷藥物前50強排名中,腫瘤治療藥物總銷售額達到了414.77億美元,成為最暢銷的藥物類別。其次是關節炎用藥、糖尿病用藥、呼吸系統藥物、血液系統藥物。

“修美樂”早在2010年便在中國獲批用于治療類風濕性關節炎,并在2010年8月初正式國內上市,在2013年CFDA又批準其用于緩解活動性強直性脊柱炎(AS)患者的相關病征和癥狀。根據南方所數據樣本醫院數據顯示,2014年阿達木單抗在我國16城市樣本醫院銷售規模達到2051萬元,同比增幅9%。阿達木單抗在我國只有進口品種,“修美樂”處于壟斷地位。
2015年共有2兩企業申報阿達木單抗注射液,治療用生物制品2類,處于臨床試驗申請階段。隨著我國生物工程產業已形成規模,抗體類藥物技術逐漸成熟,相信阿達木單抗國產品的問世不會太遙遠。
2012年10月,Enbrel專利到期,但安進公司贏得了一項新的專利,可以使Enbrel專利保護期延至2028年。Enbrel生物仿制藥品的成分專利(歐洲標準)在2015年就會到期。印度Cipla公司2013年已宣布推出Enbrel的首個生物仿制藥,將由中國上海CP國健藥業有限公司生產。三星bioepis也研發生產了Enbrel的生物類似物欲打開歐洲市場。
2014年樣本醫院數據顯示,依那西普銷售額2040萬元,同比增幅24%。目前國內恩利的仿制藥有中信國建的“益賽普”和賽金的“強克”,兩款藥品分別于2005年和2011年獲批。海正藥業的安佰諾(注射用重組人II型腫瘤壞死因子受體-抗體融合蛋白)于2015年初已完成產品注冊現場檢查,目前已經進入三合一綜合審評階段。國內也有其他廠家申報依那西普的生物仿制藥。
“可定”是阿斯利康公司的降血脂藥物,2007年開始進入中國市場。“可定”的專利將于2016年1月8日到期。在中國,近年來心血管疾病發病率呈明顯上升趨勢,瑞舒伐他汀鈣在中國的前景被看好,由于“可定”的專利保護范圍未覆蓋中國,因此,國內無論瑞舒伐他汀鈣原料藥還是制劑均不存在專利保護問題。截至2015年10月20日,CFDA批準的瑞舒伐他汀鈣產品批文共有25個,涉及浙江京新藥業、魯南貝特制藥等11家本土企業,其中6家獲得原料藥的生產批件,5家獲得制劑的生產批件,有膠囊及片劑。2014年-2015年10月,涉及瑞舒伐他汀的申請數量共有47條。
據標點信息樣本醫院數據庫統計分析,2014年瑞舒伐他汀國內銷售額同比增長37%。從樣本醫院市場來看,阿斯利康的原研藥“可定”占據76.51%的市場份額,其次,山東魯南貝特占據10.05%,其與廠家占比低于10%。
阿立哌唑是日本大冢制藥株式會社開發的新型非典型抗精神病藥,在歐洲的專利保護已經到期,2015年4月在美國專利到期,梯瓦和Apotex制藥的仿制該藥沖擊市場。
大冢制藥的阿立哌唑于2006年進入中國市場,以商品名“安律凡”上市銷售。2014年樣本醫院阿立哌唑用藥市場年銷售額約6648萬元,同比增長16%。成都康弘的仿制藥“博思清”樣本醫院市場占比達34.73%,上海中西藥業的“奧派”,占比為11.85%。總體來看,國產與原研藥物平分秋色。
阿比特龍(abiraterone acetate,澤珂)
強生的Zytiga在2011年上市之后一直統領市場,但安斯泰來(Astellas)和Medivation合作研發的新一代前列腺癌口服藥物Xtandi具有單獨用藥的獨特優勢,業界預測,在歐美兩大主要市場,Xtandi將顛覆Zytiga的霸主地位。
2015年5月,CFDA批準西安楊森制藥的 “澤珂”(Zytiga)在中國生產銷售。Zytiga的活性成分醋酸阿比特龍(Abiraterone acetate)的專利到期日為2014年2月18日,專利號US 5604213。2014-2015年,國內共有10家企業申報醋酸阿比特龍的原料藥及片劑,均為3.1類藥物,處于新藥申請臨床階段,阿比特龍的國產仿制藥指日可待。
(本文僅為部分摘錄,全文詳見第27屆全國醫藥經濟信息發布會專題資料輯)
信息來源:醫藥經濟報
|