“鉻超標”鐵棒成真兇:17省市40藥企被涉案!
日期:2016/1/6
CFDA官網于12月30日發布《國家食品藥品監督管理總局關于重慶市全新祥盛生物制藥有限公司枸櫞酸鐵銨產品風險的通告(2015年第111號)》,通告稱:查明長治市三寶生化藥業有限公司等4家企業生產的復方肝浸膏片(膠囊)中檢出的高含量鉻來自于制劑生產所用原料藥枸櫞酸鐵銨,所用枸櫞酸鐵銨為重慶市全新祥盛生物制藥有限公司生產。
鐵棒成“真兇”
初步查明,重慶市全新祥盛生物制藥有限公司未對所生產的枸櫞酸鐵銨所用原料鐵的質量進行充分控制。經對櫞酸鐵銨成品及鐵原料現場抽驗,該企業生產的枸櫞酸鐵銨中檢出高含量鉻(檢出值在643—1178mg/kg),其生產所用起始物料45號鋼棒加工的鐵屑中亦檢出高含量鉻(檢出值在149—342mg/kg),存在較高風險。
17省(直轄市)40家藥企卷入風暴
重慶市全新祥盛生物制藥有限公司生產的枸櫞酸鐵銨銷往17省(直轄市)40家藥品生產企業,蒲公英整理匯總如下:
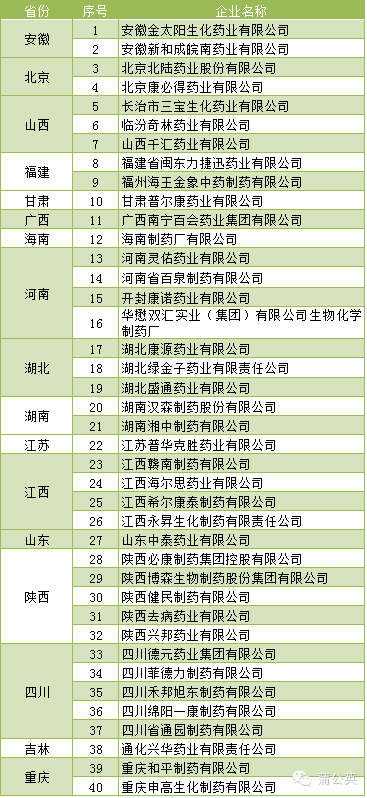
處理措施
上述40家藥品生產企業應立即停止使用重慶市全新祥盛生物制藥有限公司生產的枸櫞酸鐵銨生產藥品,并對使用該原料藥用于藥品生產的情況進行排查,查清所有有效期內藥品的品種、批次、銷售流向,召回市場銷售的產品。相關情況應于2016年1月4日前向社會公布,并報國家食品藥品監督管理總局。
國家食品藥品監督管理總局要求重慶市食品藥品監督管理局立即收回重慶市全新祥盛生物制藥有限公司枸櫞酸鐵銨的藥品GMP證書,并對該企業進一步立案調查。相關情況于2016年1月20日前報告國家食品藥品監督管理總局。
各省(區、市)食品藥品監督管理部門要監督行政區域內藥品生產企業,做好相關藥品的召回,并監督藥品經營和使用單位,配合做好召回工作。
事件回顧
12月25日,CFDA官網發布了《關于長治市三寶生化藥業有限公司等4家企業復方肝浸膏片(膠囊)檢出高含量鉻的通告(2015年第106號)》,通告稱:近日,在國家藥品抽驗中,經西安市食品藥品檢驗所檢驗,發現標示為長治市三寶生化藥業有限公司生產的復方肝浸膏片(8批)、山東中泰藥業有限公司生產的復方肝浸膏片(3批)、陜西博森生物制藥股份集團有限公司生產的復方肝浸膏膠囊(2批)、重慶申高生化制藥股份有限公司生產的復方肝浸膏膠囊(1批)檢出含有鉻成分(膠囊殼鉻含量符合規定),有10個批次檢出值在300—1200mg/kg,存在安全風險。
蒲公英微信第一時間發布了文章《這次與毒膠囊無關!復方肝浸膏片(膠囊)鉻含量超標原因分析(附73家復方肝浸膏企業名單)》,當時分析可能是“肝浸膏”引入導致鉻超標,不過,現在事實已查明,這次要為國家局的行動點贊:通報向公眾發布及時,調查迅速,原因明確,處理果斷!
===============================
附國家局通告:

國家食品藥品監督管理總局關于重慶市全新祥盛生物制藥有限公司枸櫞酸鐵銨產品風險的通告(2015年第111號)
2015年12月30日
經國家食品藥品監督管理總局調查組現場檢查,查明長治市三寶生化藥業有限公司等4家企業生產的復方肝浸膏片(膠囊)中檢出的高含量鉻來自于制劑生產所用原料藥枸櫞酸鐵銨,所用枸櫞酸鐵銨為重慶市全新祥盛生物制藥有限公司生產。現將有關事項通告如下:
一、初步查明,重慶市全新祥盛生物制藥有限公司未對所生產的枸櫞酸鐵銨所用原料鐵的質量進行充分控制。經對櫞酸鐵銨成品及鐵原料現場抽驗,該企業生產的枸櫞酸鐵銨中檢出高含量鉻(檢出值在643—1178mg/kg),其生產所用起始物料45號鋼棒加工的鐵屑中亦檢出高含量鉻(檢出值在149—342mg/kg),存在較高風險。
二、重慶市全新祥盛生物制藥有限公司生產的枸櫞酸鐵銨銷往40家藥品生產企業,分別是:安徽金太陽生化藥業有限公司、安徽新和成皖南藥業有限公司、北京北陸藥業股份有限公司、北京康必得藥業有限公司、長治市三寶生化藥業有限公司、福建省閩東力捷迅藥業有限公司、福州海王金象中藥制藥有限公司、甘肅普爾康藥業有限公司、廣西南寧百會藥業集團有限公司、海南制藥廠有限公司、河南靈佑藥業有限公司、河南省百泉制藥有限公司、湖北康源藥業有限公司、湖北綠金子藥業有限責任公司、湖北盛通藥業有限公司、湖南漢森制藥股份有限公司、湖南湘中制藥有限公司、華懋雙匯實業(集團)有限公司生物化學制藥廠、江蘇普華克勝藥業有限公司、江西贛南制藥有限公司、江西海爾思藥業有限公司、江西希爾康泰制藥有限公司、江西永昇生化制藥有限責任公司、開封康諾藥業有限公司、臨汾奇林藥業有限公司、山東中泰藥業有限公司、山西千匯藥業有限公司、陜西必康制藥集團控股有限公司、陜西博森生物制藥股份集團有限公司、陜西健民制藥有限公司、陜西去病藥業有限公司、陜西興邦藥業有限公司、四川德元藥業集團有限公司、四川菲德力制藥有限公司、四川禾邦旭東制藥有限公司、四川綿陽一康制藥有限公司、四川省通園制藥有限公司、通化興華藥業有限責任公司、重慶和平制藥有限公司和重慶申高生化制藥有限公司。
上述40家藥品生產企業應立即停止使用重慶市全新祥盛生物制藥有限公司生產的枸櫞酸鐵銨生產藥品,并對使用該原料藥用于藥品生產的情況進行排查,查清所有有效期內藥品的品種、批次、銷售流向,召回市場銷售的產品。相關情況應于2016年1月4日前向社會公布,并報國家食品藥品監督管理總局。
三、國家食品藥品監督管理總局要求重慶市食品藥品監督管理局立即收回重慶市全新祥盛生物制藥有限公司枸櫞酸鐵銨的藥品GMP證書,并對該企業進一步立案調查。相關情況于2016年1月20日前報告國家食品藥品監督管理總局。
四、各省(區、市)食品藥品監督管理部門要監督行政區域內藥品生產企業,做好相關藥品的召回,并監督藥品經營和使用單位,配合做好召回工作。
食品藥品監管總局
2015年12月30日

關于長治市三寶生化藥業有限公司等4家企業復方肝浸膏片(膠囊)檢出高含量鉻的通告(2015年第106號)
2015年12月25日
近日,在國家藥品抽驗中,經西安市食品藥品檢驗所檢驗,發現標示為長治市三寶生化藥業有限公司生產的復方肝浸膏片(8批)、山東中泰藥業有限公司生產的復方肝浸膏片(3批)、陜西博森生物制藥股份集團有限公司生產的復方肝浸膏膠囊(2批)、重慶申高生化制藥股份有限公司生產的復方肝浸膏膠囊(1批)檢出含有鉻成分(膠囊殼鉻含量符合規定),有10個批次檢出值在300—1200mg/kg,存在安全風險。
復方肝浸膏片(膠囊)屬補血制劑,主要成分為鐵元素,沒有規定鉻的限量標準。為保障公眾用藥安全,國家食品藥品監督管理總局要求山西省、山東省、重慶市、陜西省食品藥品監督管理局監督上述4家企業立即停止生產,查清復方肝浸膏片(膠囊)生產、銷售情況和具體銷售流向并及時向社會公布相關信息,召回市場全部批次產品,并報告產生問題的原因。調查處置情況于2016年1月10日前報告國家食品藥品監督管理總局。
各省(區、市)食品藥品監督管理部門要監督行政區域內的相關企業及單位立即停止銷售和使用上述企業生產的復方肝浸膏片(膠囊),并配合做好召回工作,發現患者服用該藥后出現不良反應及時報告。
國家食品藥品監督管理總局已組織調查組進行調查,調查情況及時向社會公布。
食品藥品監管總局
2015年12月25日
小貼士:
復方肝浸膏片及復方肝浸膏膠囊臨床上主要用于治療缺鐵性貧血。該品種的主要成分為肝浸膏、枸櫞酸鐵銨及B族維生素。
鉻是人體必需的微量元素之一。原國家食品藥品監督管理局發布的《營養素補充劑與審評規定(試行)》中規定三價鉻用量范圍為15-150μg/天。六價鉻對人體危害較大。
國家食品藥品監督管理總局通告的4家生產企業生產的復方肝浸膏片及復方肝浸膏膠囊中鉻檢出值在300-1200mg/kg之間,目前檢測方法尚不能區分其中鉻為三價鉻還是六價鉻。按照藥物服用量,即使按檢出值為300mg/kg計算,日攝入鉻的劑量也達到1350μg/天。
信息來源:蒲公英
|