80家藥企被責令停產
日期:2016/1/6
導讀
2016年1月4日,青海市藥監局發布通知,責令青海青藏雪山資源開發有限公司等5家藥品生產企業停止生產。
2015年12月31日,安徽省藥監局發布通知,對未通過新修訂藥品GMP認證企業停產檢查,其中75家藥企未通過新版GMP認證。
根據國家藥監總局《關于切實做好實施藥品生產質量管理規范有關工作的通知》(食藥監藥化監〔2015〕277號)精神,自2016年1月1日起,未通過《藥品生產質量管理規范(2010年修訂)》(以下簡稱藥品GMP)認證的藥品生產企業(或生產車間)一律停止生產。由于青海青藏雪山資源開發有限公司、青海未來格薩爾王藏藥制藥有限公司、青海君吒藥業有限公司、青海央宗藥業有限公司、青海瑞誠工貿有限責任公司逾期未通過新版GMP認證。為確保藥品質量,青海市藥監局經研究決定,責令上述5家藥品生產企業自2016年1月1日起停止生產。
根據國家藥監總局《關于未通過藥品生產質量管理規范(2010年修訂)認證企業停止生產和下放無菌藥品認證有關事宜的公告》(2015年第285號)的要求,未通過藥品GMP認證的藥品生產企業,自2016年1月1日起全部停止生產。
安徽省局要求加大對藥品生產企業的監督檢查力度,確保未通過新修訂藥品GMP認證的藥品生產企業、車間和生產線自2016年1月1日起一律停止藥品生產,逐一進行現場檢查,確認其保持停產狀態;一旦發現未按規定停產的,按照《中華人民共和國藥品管理法》及相關規定嚴肅查處;對停產企業的原輔材料、包裝材料等進行登記并采取切實有效的管控措施,對特殊藥品應嚴格監管到位,嚴防流弊。從表格統計得知,此次停產的藥品生產企業包括安徽國正藥業股份有限公司、安徽威爾曼制藥有限公司、合肥華威藥業有限責任公司等75家,認證范圍涵蓋等片劑、硬膠囊劑、顆粒劑、口服溶液劑、外用溶液劑、中藥飲片、醫用氧等。其中,合肥市12家,淮北3家、毫州29家、宿州4家、蚌埠3家、阜陽1家、淮南3家、滁州3家、馬鞍山3家、蕪湖4家、宣城3家、銅陵1家、池州市1家、安慶市1家、黃山市2家。
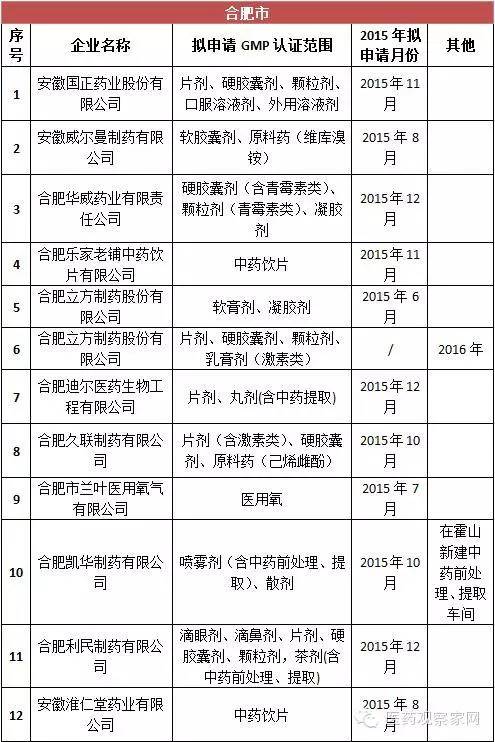
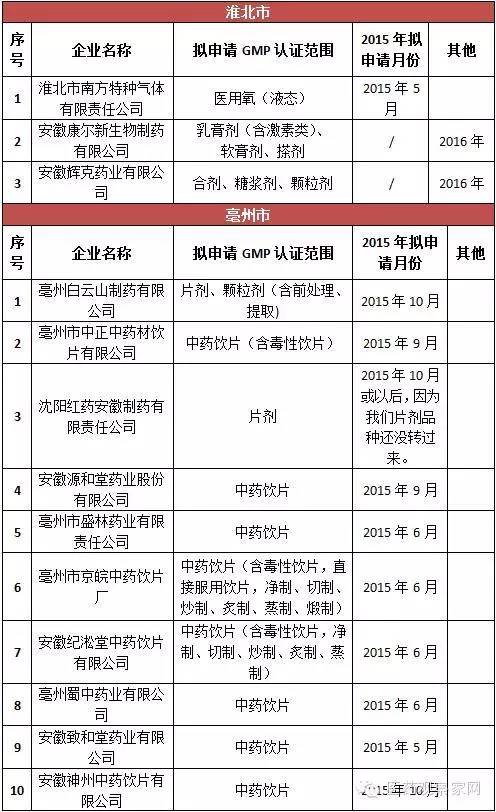
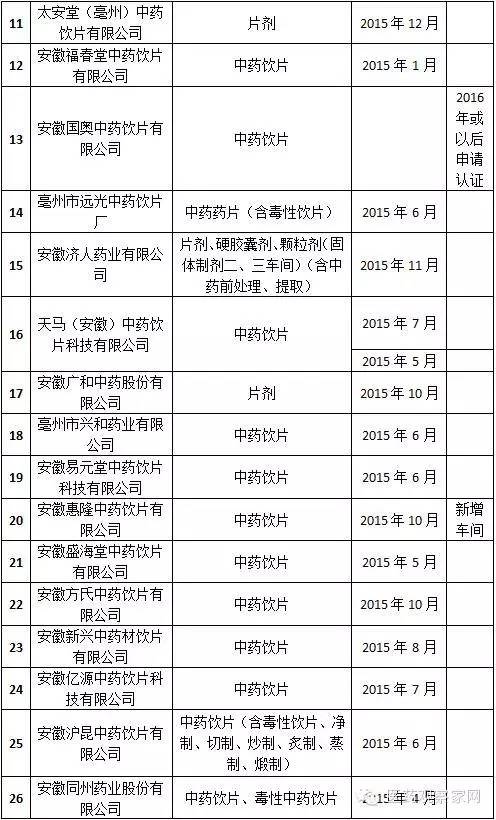
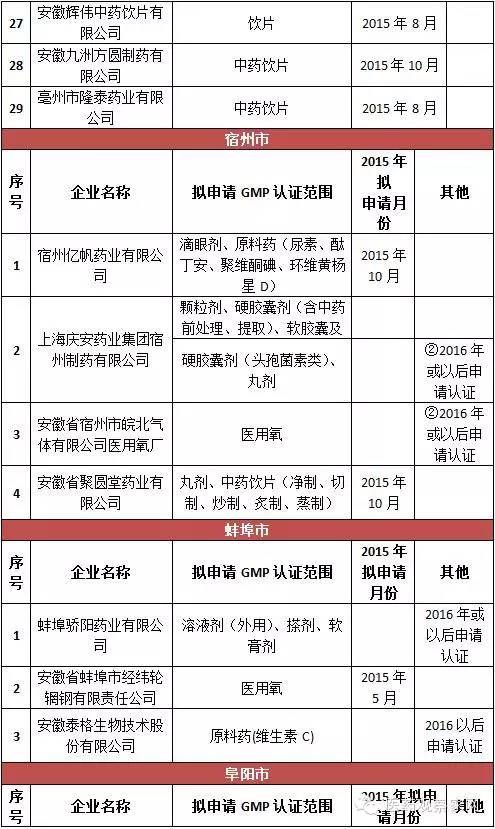
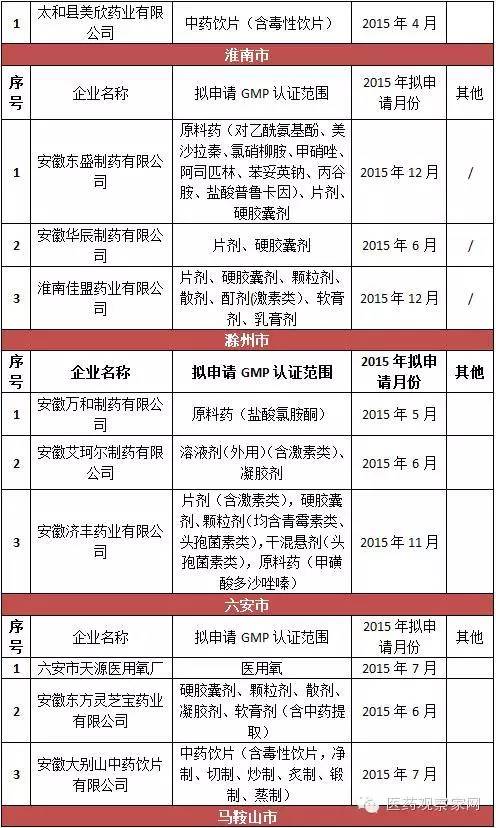

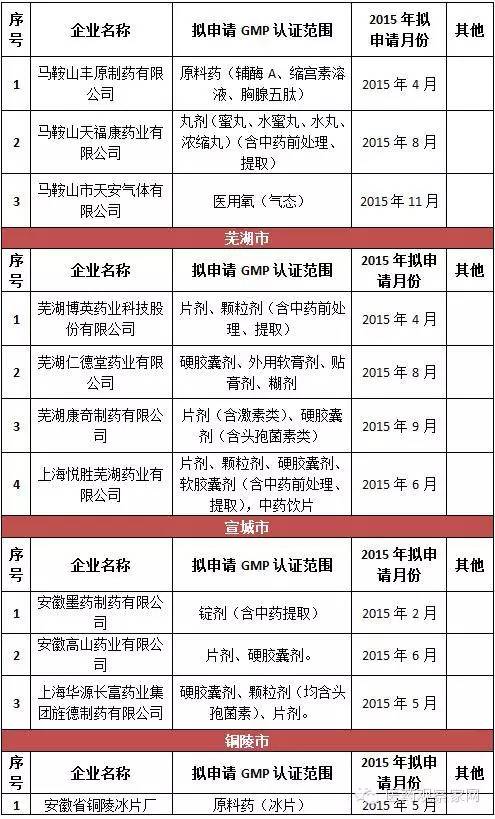
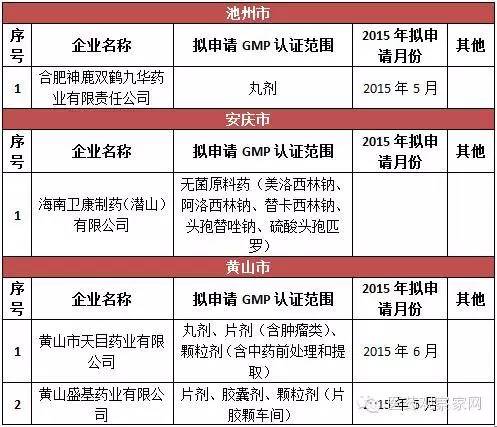
據悉,安徽省約有藥品生產企業337家。其中,持有藥品生產許可證的制藥企業162家,中藥飲片企業151家,醫用氧(液態)企業24家。3年來,全省共有230多家企業通過了新版GMP認證。其中,30家無菌藥品生產企業,全部通過新版GMP認證。亳州市三友醫用氧氣有限公司、安徽省科健中藥飲片有限公司等15家企業正在審批過程中;省食品藥品審評認證中心正在辦理上海賽睿宿州藥業、安徽東方靈芝寶藥業、安徽協和成藥業等26家藥企的新版GMP認證。

省食品藥品審評認證中心正在辦理:

信息來源:醫藥觀察家網
|