【黑榜】第一家涉“疫苗案”企業GSP被撤銷!所涉12種疫苗公布!絕不姑息!
日期:2016/3/24
3月22日山東食藥監局發布通告,山東兆信生物科技有限公司嚴重違反《藥品經營質量管理規范》規定,依據國家總局《藥品經營質量管理規范認證管理辦法》第四十五條規定,依法撤銷其《藥品經營質量管理規范認證證書》。這家企業正是CFDA此前公布的9家藥品批發企業涉嫌虛構疫苗銷售渠道之一。
文│李靜芝
山東非法經營疫苗案繼續發酵,雷霆萬鈞。
3月21日晚,CFDA連發兩條公告:《對河北省衛防生物制品供應中心等9家藥品批發企業立即開展調查的通知》和《食品藥品監管總局公安部國家衛生計生委關于共同做好非法經營疫苗案件查處工作的通知》。一方面公布了涉案的9家藥品批發企業名單,并要求各省3月25日提交調查結果;另一方面加大對該案的聯合調查力度,各個部門協同作戰。
《對河北省衛防生物制品供應中心等9家藥品批發企業立即開展調查的通知》根據山東濟南非法經營疫苗案查扣藥品的數據分析,公布了9家藥品批發企業涉嫌虛構疫苗銷售渠道,可能是造成涉案疫苗流入非法渠道的主要責任者名單。
名單如下:
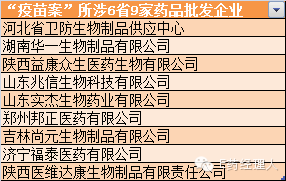
同時要求各有關省食品藥品監管局對上述9家藥品批發企業立即開展調查,徹底查清其虛構銷售產品的真實流向,查實存在違法違規行為的,立即立案查處,依法嚴肅懲處。涉及其他企業的也必須追查到底。并規定3月25日上報調查結果。由總局統一向社會公開。
另外,《食品藥品監管總局公安部國家衛生計生委關于共同做好非法經營疫苗案件查處工作的通知》,規定每日17時分別向食品藥品監管總局、公安部、國家衛生計生委匯報調查進展。
具體內容是:
一、地方各級食品藥品監管、公安和衛生計生部門要立即成立聯合工作組,統一指揮、密切配合,切實落實落地查人責任,共同做好非法經營疫苗案件涉案產品處置和案件查辦工作。
二、食品藥品監管和公安部門應當密切配合,根據山東省公布的涉案嫌疑人員名單和協查線索,對涉及本地區的嫌疑人盡快核實身份,及時查明疫苗購銷情況。對屬于銷售上線的,應當查明銷售單位和人員以及銷售的品種、生產企業、批號、數量等情況;對屬于購進下線的,應當查明購進單位和人員以及購進的品種、生產企業、批號、數量、銷售去向等情況。食品藥品監管、公安和衛生計生部門應當對非法購銷疫苗的企業、機構和個人,根據事實和情節依法嚴肅查處。查處情況要逐案及時上報上級主管部門。
三、食品藥品監管和公安部門對查實醫療衛生機構購入、使用涉案疫苗的,應當及時通報同級衛生計生部門。衛生計生部門應當配合食品藥品監管部門迅速查明疫苗最終去向及使用情況,要做好風險評估并采取相應措施,切實保護公眾健康。
四、各級聯合工作組應當及時匯總工作進展情況,每日逐級向上級聯合工作組上報。省級聯合工作組需將本地區情況匯總后,于每日17時前分別報食品藥品監管總局、公安部、國家衛生計生委。案件查辦中如遇到問題,應當及時向上級部門請示,并向所在地人民政府報告。
根據3月20日山東省食藥監局發布的信息,此次“山東非法經營疫苗案”所涉及的產品包括12種疫苗、兩種免疫球蛋白和一種治療性生物制品。
具體名單如下:

信息來源:E藥經理人
|